选择性必修三 第五章 原子核 参考资料
1.物理学家
(1)贝克勒尔
贝克勒尔是法国物理学家。他 1895 年任巴黎高等工业学校物理学教授,1897 年成为科学院院士。伦琴发现了 X 射线后,贝克勒尔在研究这种不可见辐射与可见光之间的联系时发现,某些铀盐能放出不可见的射线,使包在厚黑纸中的胶片感光,这就是后来被称为放射性的现象。1899 ~ 1900 年,他测定了 β 射线在电场和磁场中的偏转,证明了 β 射线就是电子束。1901 年,他又报告了辐射的生理效应:他因内衣口袋里装着放射样品而受到了灼伤。贝克勒尔因发现放射性,与居里夫妇一起,荣获 1903 年诺贝尔物理学奖。
(2)玛丽·居里
玛丽·居里是法国物理学家和化学家。她是放射性学说的奠基人之一,原籍波兰,出生于华沙。玛丽·居里 1891 ~ 1894 年在巴黎大学学习,1895 年和物理学家皮埃尔·居里结婚,夫妻共同致力于科学研究工作。皮埃尔的早期贡献有:确定了磁性物质的转变温度,建立了居里定律,发现了晶体的压电现象。
1896 年贝克勒尔发现了放射性。居里夫妇对铀、钍等矿物的放射性进行了研究,并从大量沥青铀矿中分离出放射性更强的物质,于 1898 年发现了两种元素:钋和镭。由于发现放射性,居里夫妇和贝克勒尔共获 1903 年诺贝尔物理学奖。
1906 年,皮埃尔因车祸不幸逝世。玛丽接任了她丈夫在巴黎大学的物理学教授职位,成为该校第一位女教授。1910 年,她和法国化学家德别爱尔诺一起分析出纯镭元素,并确定了它的原子量和在元素周期表中的位置。她还测出了氡和其他许多放射性元素的半衰期,整理出放射性元素衰变的系统关系。由于这些重大成就,居里夫人又荣获 1911 年诺贝尔化学奖。
居里夫人研究了放射性辐射对人体细胞的影响,第一个在医学上利用了放射性。1922 年被选为医学研究院会员,此后她专心致力于化学和放射性物质在医学上的应用研究。
(3)约里奥—居里夫妇
F.约里奥—居里和他的妻子 I.约里奥—居里是法国物理学家。1932 年他们在云室实验中取得第一张同时产生的正负电子对的照片。他们对中子的发现也作出了重要贡献。1932 年 1 月,曾就一种强穿透性粒子发表论文,同年 2 月,经查德威克研究,确定为中子。1934 年,他们用钋产生的 α 粒子轰击铝,产生出中子和正电子,生成放射性磷,首次获得人工放射性物质。他们用同样方法又制成许多其他放射性物质,并发现放射性同位素在医学和生物学上有广泛用途,因此获得了 1935 年诺贝尔化学奖。1938 年年底,哈恩等人发现核裂变不久,约里奥—居里夫妇也独立发现了这一过程,并提出核裂变中产生的许多中子有可能发展成链式核爆炸反应。
2.对原子核结构的认识简史
早在 1815 年,英国医生兼化学家普劳特根据多数元素的原子量是氢原子量的整数倍,提出所有元素都由氢原子组成的假说。因为发现有些元素的原子量不是整数,特别是氯的原子量为 35.46 个单位,铜的原子量为 63.54 个单位,这个假说到 19 世纪末被放弃了。
19 世纪末 20 世纪初,发现了放射性现象和同位素,引起了对原子构造的新探索,也包括对原子核结构的探索。1919 年,卢瑟福发现一个 α 粒子能引起氮核的人工衰变,而衰变的产物之一是质子(即氢核)。1921 ~ 1924 年,卢瑟福和他的学生查德威克对硼、钠、铝等轻元素进行人工核反应,同样有质子分裂出来。以上事实显然说明原子核内存在质子。问题是原子核是否只有质子?当人们从元素周期表看到除氢以外,核的电荷数(原子序数)总是小于质量数时,曾假定原子核内除质子之外,还包含电子,它们的电荷量足以抵消额外质子的电荷,而电子的质量很小,不影响原子核的质量。即一个原子序数为 Z,质量数为 A 的原子核,它就是由 A 个质子和(A − Z)个电子所组成的。这就是核结构的质子—电子假说。
质子—电子假说在某些方面能初步说明各种元素的性质,如解释原子核的 α 和 β 衰变现象、核质量近似为质子质量的整数倍等。但是这一假说与许多实验事实不符,理论上也存在困难,例如,随着测量的逐渐精确,核质量愈加偏离质子—电子假说所预言的质量;束缚在核内的电子,要有上百兆电子伏的能量,而 β 衰变的电子能量只有 1 MeV 的量级,靠电子—质子之间的微弱的电磁相互作用力根本不可能使电子保持在核内。另外,例如氮 147N 核的角动量,按照质子—电子假说应为 14 个质子与 7 个电子,自旋值为 14×\(\dfrac{1}{2}\) + 7×\(\dfrac{1}{2}\) = 21×\(\dfrac{1}{2}\)(奇数个半整数),即为费米子,而通过原子光谱的超精细结构的实验测定却应为偶数个半整数,即 147N 核应为玻色子!最后,实验也测不出核内含有的电子磁矩,而只能成功地测出质子的磁矩,前者应为后者的 1 840 倍(与质量成反比)。质子—电子假说所遇到的这些巨大困难,说明了人们对微观世界认识的曲折进程。也从反面说明了质子—中子说的来之不易。
1920 年,卢瑟福提出一种猜想,预言原子核内可能存在一种质量与质子相近的中性粒子。1921 年,美国化学家哈金斯将它命名为“中子”。卢瑟福一直追寻这种粒子,但经历了 12 年后,才由他的学生查德威克找到。
中子的发现证实了卢瑟福预言的正确性,使得建立一种没有电子参与的核模型成为可能。1932 年,海森堡和苏联物理学家伊万年科各自独立地提出了原子核由质子和中子组成的假说,根据这一假说,一个原子序数为 Z 和质量数为 A 的原子核,由 Z 个质子和(A − Z)个中子组成。
核结构的质子—中子假说圆满地说明了元素的质量数和电荷数,解释了同位素以及放射性现象,使“质子—电子”假说面临的许多困难迎刃而解,因而立即被科学界普遍接受,很快成为原子核理论的基础,至今仍然是描述核的特性和结构的基础。这促进了对核作用力的研究,为粒子物理的发展开辟了道路。
人们在认识原子核结构的过程中,主要提出了五种具体的模型:气体模型、液滴模型、α 粒子模型、壳层模型、综合模型。各种模型分别适用于核现象的一个特定方面,但迄今还没有哪一个模型能恰当地、圆满地描述从放射性衰变到核反应和裂变的广阔范围里的一切现象。此外,还须进一步研究质子—质子、质子—中子、中子—中子这三种相互作用,以便说明原子核的主要性质。
有些实验表明,核内除有质子和中子外,还可能存在其他粒子,例如,当核被高能激发时出现 π 介子;1953 年发现了含有 Λ 超子的超核,近些年来又发现了含有超粒子的超核。这些问题还和迅速发展的“基本粒子”物理紧密相关。因此,人类仍然需要对原子核的结构及其内部运动规律进行不断地探索。
3.用云室观察 α 粒子的径迹
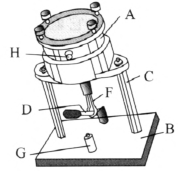
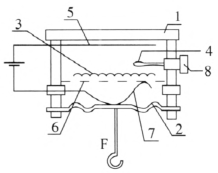
J 2553 型威耳逊云室外形如图 5–1 所示。密闭容器(云室)A 装在底座 B 的支架 C 上,杠杆 D 通过拉杆 F 能使云室的底上下运动,G 为限位柱,孔 H 供装入放射源用。云室 A 的内部结构如图 5–2 所示。
使用方法:
(1)由孔 H 用吸管向云室中的呢绒 3 上均匀地滴洒约 1 mL 的稀释酒精(60 % 工业酒精和 40 % 水混合),如外界气温低于 15 ℃ 则酒精不必稀释。
(2)将放射源 4(含镭或钍)的杆插到螺栓 8 上,由孔 H 放入云室内。拧紧螺栓,使之密封,这样,云室中就充满了饱和蒸气。
(3)将 J1205 型高压电源的 300 V 直流电源接到云室的接线柱上,正极通金属丝 5,负极经过弹簧片 7 通金属网 6,使 5 和 6 间形成电场。放射源放出的粒子会使云室中形成大量离子分布在空间中,这电场的作用就是将这些离子吸引到电极上,就不会影响观察新放出的粒子径迹。
(4)用强光由侧面射入云室。但光源不可距离云室太近,以免引起云室内气体形成热对流。
(5)用手将杠杆 D 迅速下压,拉杆 F 使云室的底 2 向下运动,云室中气体绝热膨胀而降温,蒸气变为过饱和,这一瞬间通过透明上盖 1 可看到若干条由放射源向四周呈辐射状的细小液滴串,显示出放射源射出的 α 粒子的径迹。这时弹簧片随云室的底下移而与金属网分离,空间中的电场消失,不致影响 α 粒子的运动。
(6)放开杠杆,经过 30 ~ 60 s,待云室中蒸气恢复平衡后,可再次向下压杠杆观察径迹。
注意事项:
(1)如云室密封不严就不出现径迹,应将上盖压圈上的四个螺丝再拧紧些。
(2)调节限位柱 G 的高度可改变云室的膨胀比 K,一般 K 值取 1.23 ~ 1.26 为宜。K 过小则不出现径迹,K 过大则会出现一片白雾。
(3)如上盖玻璃 1 的下表面附着露珠影响观察,应将螺栓 8 拧下,压几次杠杆将过多的蒸气排出一些。操作时要用纱布挡住孔 H,避免尘土吸入云室中。
(4)用毕将放射源放回铅罐或玻璃管中保藏。放射源不要接触手和其他物体,实验后要用热水肥皂洗手。
(5)J1205 型高压电源关断开关后,其输出端内部的电容器仍充有电荷,人同时触及其两极,会产生触电的感觉。可将两极导线短路几下使之放电。
4.衰变定律
实验表明,在时间 dt 内,放射性元素衰变的原子核数 dN 跟放射性元素的原子核数 N 以及 dt 成正比。
\[{\rm{d}}N = - \lambda N{\rm{d}}t\tag*{①}\]
式中 λ 是比例恒量,叫作衰变恒量,表征放射性元素衰变的快慢。式中出现的负号是由于放射性元素的原子核数目是随着时间的增加而减少的。把①式改写成
\[\dfrac{{{\rm{d}}N}}{{{\rm{d}}t}} = - \lambda {\rm{d}}t\]
积分得
\[\ln N = - \lambda {\rm{d}}t + C\]
用 N0 表示 t = 0 时放射性原子核的个数,代入上式得 C = lnN0,因此
\[\ln N = - \lambda {\rm{d}}t + \ln {N_0}\]
即
\[\ln \dfrac{N}{{{N_0}}} = - \lambda t\]
所以
\[\dfrac{N}{{{N_0}}} = {e^{ - \lambda t}}\]
\[N = {N_0}{e^{ - \lambda t}}\tag*{②}\]
由于放射性元素的质量 m 和它所包含的原子核数成正比,所以
\[m = {m_0}{e^{ - \lambda t}}\tag*{③}\]
式中 m0 为 t = 0 时放射性元素的质量。②和③式叫作放射性元素的衰变定律。
习惯上常用半衰期来表示放射性元素衰变的快慢。半衰期就是原有的原子核数衰变掉一半所经历的时间,用 τ 表示。当 t = τ 时,由②式得
\[\frac{1}{2}{N_0} = {N_0}{e^{ - \lambda \tau }}\]
所以
\[\lambda \tau = \ln 2\]
\[\tau = \dfrac{{\ln 2}}{\lambda } = \dfrac{{0.693}}{\lambda }\]
可见半衰期是由衰变恒量决定的一个恒量。不同的放射性元素,它们的半衰期也不同,半衰期越短的放射性越强。
5.γ 射线探伤法
γ 射线探伤法是用 γ 射线检验金属材料与工件内部缺陷的方法。通常采用射线照相法。让 γ 射线穿过被检查的工件,在工件后面放上底片,并尽量与工件贴紧。穿过缺陷部分到达底片的射线比穿过正常部分到达底片的射线,强度要大,在显像后的底片上会显示出黑色区域,用这种方法可以发现工件内部缺陷,并确定其大概的形状和位置。
为了使拍照的影像清晰,放射源与工件的距离应比工件大。还可以在底片前面放一张重元素屏,例如铅屏(称为增感屏),因为穿过工件的 γ 射线会在屏中产生光电子和康普顿电子,这些次级电子可以增强底片的感光。增感屏的最佳厚度,主要由 γ 射线的能量决定,也跟所用底片的性质有关。
γ 射线探伤经常采用的放射源有 60Co、137Cs、192Ir 等。不同放射性核素发出的 γ 射线能量不同。低能射线探测的灵敏度高,但探伤厚度不及高能射线。60Co 的 γ 射线能量为 1.17 MeV 和 1.33 MeV,可探测 5 ~ 30 cm 的钢铁制品;192Ir 的 γ 射线能量为 0.137 MeV 和 0.651 MeV,可检验 1 ~ 6 cm 的钢铁制品。
6.放射性示踪法
由于放射性核素不断发出辐射,无论它运动到哪里,都很容易用探测器探知它的下落,因此可以用作示踪物来辨别其他物质的运动情况和变化规律。这种放射性示踪物称为示踪原子或标记原子。
1911 年,赫维西第一次使用了放射性示踪物。为了确定女房东是不是把星期天剩下的馅饼掺到后几天的膳食中,他把一些放射性钍放到新做好的馅饼中,到了星期三,借助于验电器指给女房东看,在蛋奶酥中含有放射性物质。不久,他就把示踪法引入到研究工作中去。
自那以后,放射性示踪技术已有长足进步:放射性核素的数目及其有效性大大增加了,探测方法的灵敏度及其在能量的选择性方面都有很大改进。例如,第 101 号元素钉(Md),只要有 20 个原子,就能把它鉴别出来。因此,放射性示踪技术,在工农业生产、医疗卫生和科学研究等方面都有广泛的应用。例如,可以将放射性同位素引入待研究的机械材料中去,在制成的机件运转时,收集磨损下来的碎屑和落下的润滑油,定时测量它们的放射性,就可以确定机件的磨损情况。又如,用放射性杂质代替寻常杂质,扩散到半导体中,然后逐层磨下,测量其放射性强度,就可以了解杂质扩散的情况。在农业上,可以用放射性示踪研究作物对肥料的吸收情况:把放射性颗粒状磷肥放到作物根旁土壤中,15 ~ 20 min,叶片上就有放射性磷出现,观察放射性增加的速度,就能估计作物吸收磷肥的速度。在医学和生命科学的研究方面,把用放射性核素标记的物质 A 引入动物体,经过一段时间,从排出物或组织中分离出另一化合物 B,含有相当数量的上述标记核素,即可确定 A 在动物体内可以转变为 B。例如,将 14C 标记的糖喂给大鼠,发现从其脂肪中分离出来的脂肪酸有很强的放射性,就证明了糖在动物体内可以变成脂肪这一很重要的代谢规律。也可以用放射性标记某种物质,追踪这种物质在动物体内转移和移动的速度,研究其吸收、摄取、浓集、分布、分泌、排泄以及药物作用原理等问题。
放射性示踪的应用,隐含着两个假定:一是放射性核素和它的稳定同位素化学性质相同;二是研究对象的化学特性不受放射性衰变的影响。第一个假定,仅当同位素的质量效应很重要时才是不正确的,这种情况只在氕—氘—氚互相取代时才会发生。第二个假定,只要示踪物的浓度很小就是正确的。
7.放射性测定年代
应用放射性核素的衰变规律,可以测定矿石、地层的生成年代,也可以测定某些古文物的年代和古生物遗骸的死亡年代。前者可用铀铅法,后者用 14C 法。
铀铅法 238U 的半衰期为 4.5×109 年,它的最终子体是稳定的 206Pb。假定矿石在生成时不含铅,单位质量中 238U 的原子数为 N0(238U),λ 为 238U 的衰变常量,矿石的年龄为 t,则目前每单位质量中,238U 的原子数目为 N(²8U)= N0(238U)e− λt;206Pb 的原子数目为 N(206Pb) = N0(238U)− N(238U)− Nʹ,Nʹ 为单位体积中所有 238U 的放射性子体的原子数目。当 t 很大(超过 105 年)时,Nʹ ≪ N(206Pb),则有 N(206Pb)= N0(238U)− N(238U)= N(238U)(eλt − 1)。由此可得 t = \(\dfrac{1}{\lambda }\ln \left[ {\dfrac{{N{(^{206}}{\rm{Pb}})}}{{N{(^{238}}{\rm{U}})}} + 1} \right]\)。所以,测出矿石样品单位体积中 206Pb 原子数与 238U 原子数的比,就可以知道矿石的年龄。
14C 法 在碳元素中除了含有大量稳定的 12C 和 13C 外,还含有微量的放射性同位素 14C,半衰期为 5 730 年,它是宇宙射线中的中子穿过大气层时与空气中的 14N 核碰撞发生核反应生成的,即 147N + 10n → 146C + 11H。
宇宙射线不断地射到地球上来,14C 不断地产生又不断地衰变,结果大气中 14C 的含量保持不变。大气中的 14C 与氧化合生成放射性二氧化碳 14CO2,通过光合作用进入植物体。动物以植物为食,14C 又进入动物体。因此,在生物体内 14C 与非放射性碳的含量比与大气中二氧化碳里两者的比相同。生物体死亡以后停止了与外界的物质交换,体内原有的 14C 只能不断地衰变而得不到补充。因此,从古代生物遗骸中 14C 与非放射性碳的含量比,就可以求出它死亡的年代 t。用 λ 表示 14C 的衰变常量,A0 = λN0 表示处于交换运动中的 14C 的放射性活度,A = λN 表示所测样品的 14C 的放射性活度,仿照铀铅法的推理,则有 t = \(\dfrac{1}{\lambda }\ln \dfrac{{{A_0}}}{A}\)。
构成生物体的碳中,14C 的含量极少,12C 与 14C 原子含量的比为 1012∶1.2。因此,测定 14C 的放射性相当困难,需用特殊的技术与装置。
8.辐射防护
核辐射的生物效应主要由于电离作用对生物分子的破坏。因此,一切致电离辐射——能直接引起电离的 α 粒子、β 粒子和质子,能间接引起电离的 γ 射线和中子,都可能成为伤害人体的来源。
致电离辐射在人体某种组织中造成的伤害程度,首先取决于辐射在该组织中沉积的能量。其次,能量沉积的距离(或体积)也是重要的。如果能量在短距离内沉积,它对某种组织的伤害大于沉积距离大的情况。例如,α 粒子在人体组织中的射程非常短,就是说它们在短距离内沉积能量,所以进入体内的放射性源发出的 α 粒子所造成的伤害,比 γ 射线源(不管是体内的还是体外的)沉积同样能量所造成的伤害大。
外部照射的损伤主要由体外辐射源发出的 γ 射线所引起。α 和 β 粒子几乎不会引起损伤,除非它的源非常接近人体或就在皮肤表面上。而以各种方式进入体内的 α 粒子、β 粒子、γ 射线或中子的源,则引起内部照射。这时,人体就将连续不断地遭受辐射照射,放射性物质的量只能靠自然衰变和人体排泄而减少。
某些元素天然倾向于集中在特定的组织或器官中,这些元素的放射性同位素的行为与其稳定的同位素一样。例如,所有碘的同位素都倾向于聚集在甲状腺中,钙的同位素则沉积在钙化的骨组织中。锶、钡和镭与钙的化学性质类似,它们具有置换骨中钙的倾向。钚如果溶入血液中则将部分地沉积在某些骨骼表面或肝脏中,存留相当长的时间。比较难溶解的钚化合物,如二氧化钚,吸入肺之后,可以存留数年之久。
微弱的放射性照射对人体并无损伤。人们是经常处于射线的照射之下的。自然界存在的 14C、40K、226Ra 等放射性元素,在人体内不断地新陈代谢,并发出射线。但人们对此都能自然地适应,并不影响健康。只有超过一定剂量的照射,才会造成伤害:能引起各种放射病,重者可以致死;远期效应可引起各种恶性肿瘤、不育甚至早亡。
对体外照射的防护应从以下四个方面着手:①在使用放射性物质时(如在实验工作中)用量要尽可能少。②受照射的时间尽可能短,不要在放射性物质的周围做不必要的停留,用放射性物质进行的操作,力求熟练、迅速。③与放射性源的距离尽可能远,如操作时利用各种夹具或进行远距离操纵。④屏蔽,常用的材料有铅、铁、水泥、砖、石、泥土、硼酸、石蜡、铝、铅玻璃、有机玻璃、水和溴化锌水溶液等。
对不同的放射性粒子,可采用不同的措施。Α 粒子射程很短,工作时只要戴上手套,不直接去摸放射性物质就可以了。Β 射线比 α 粒子的贯穿能力强,在空气中的射程可达数米,但它容易被不太厚的铝层、铜片、有机玻璃或玻璃所吸收。不过原子量较大的物质,例如铅,一般不适于做 β 射线的屏蔽物,特别是对于高能量的 β 射线更不适宜,因为它们较易引起贯穿力很强的X 射线(轫致辐射)。γ 射线的贯穿能力比 α、β 射线大得多,要选用原子序数大、密度大的材料,如铁、铅、铅玻璃等来屏蔽。考虑到经济实用,也可用混凝土、水等廉价材料。中子的防护可归结为快中子的减速和慢中子的吸收。中子的减速用轻元素,最好的是氢,实用上多采用水、石蜡做中子的慢化剂。氢也是比较好的吸收剂,但效果不如锂和硼,一般常用硼酸水溶液做吸收剂。
对内照射的防护,必须避免放射性物质进入体内和污染身体。要禁止在可能存在放射性污染的地区抽烟、进食或饮水。通风系统的设计必须使空气总是从辐射水平较低的区域流向辐射水平较高的区域。尘埃也要加以控制,最好用真空除尘,清扫时应有足够湿度,以防止尘埃飞扬。在空气尘埃难以避免的区域内工作时,应戴适当的面具。对出入可能存在放射性污染区域的人员,应提供一次性使用的工作服、手套和鞋套;这些物品应留在规定的出口,根据情况进行去污或另做处理。对离开现场的工作人员要仔细进行放射性监测。
9.粒子间的相互作用
物质世界运动变化多样性的根源在于自然界存在着四种基本相互作用,即强相互作用、电磁相互作用、弱相互作用和引力相互作用。
强相互作用 存在于重子、介子等强子之间的基本相互作用。核子之间的核力是它的一个典型实例。强相互作用是一种短程力,作用范围为 10−15 m 量级,作用强度约为电磁相互作用的 102 倍。目前,对强相互作用的机制还不清楚。近年来发展的量子色动力学(QCD)能解释强相互作用的一些问题。这个理论认为强相互作用是通过胶子传递的。实验上已观察到胶子存在的迹象,但还没有直接的证据证明胶子的存在。
电磁相互作用 这是目前了解得最清楚的一种相互作用,量子电动力学(QED)可以对它进行精确的计算。电磁相互作用是一种长程力,作用于所有微观或宏观带电或带磁矩的物体之间。大到天体,小到 10−18 m 范围内,理论计算都跟实验事实符合得很好。量子电动力学认为,电磁相互作用是由电磁场的量子——光子传递的。
弱相互作用 广泛存在于轻子和轻子间、轻子和强子间、强子与强子间的一种基本相互作用。原子核的 β 衰变是它的一个实例。弱相互作用也是一种短程力,作用范围比强相互作用还要短,作用强度约为强相互作用的 10−6 倍。弱相互作用是通过质量很重的中间玻色子 W± 和 Z0 传递的,它们的质量分别为:mW±=(80.9±1.5)GeV,mz0 =(95.6±1.4)GeV。
引力相互作用 支配着宏观物体运动变化,例如,天体运动规律的一种长程力。在微观领域里,引力相互作用远远弱于其他三种相互作用,以致实际上无法检验在微观领域里万有引力定律是否仍然正确。例如,根据万有引力定律考虑两个质子间的引力相互作用与它们间的强相互作用的强度之比仅为 10−38。理论上,传递引力相互作用的量子是引力子。目前,实验上尚未发现引力子的存在。
现代的量子场论认为,每一种粒子都有一种与之对应的场存在。场没有不可入性,各种不同粒子的场互相重叠,充满整个空间。场能量的最低态称为基态;场的激发态表现为出现相应的粒子,不同的激发态表现为粒子数目和状态的不同。场处于基态时没有粒子出现。所有的场都处于基态时,就是物理真空。所以场是比粒子更基本的物质形态。无论是处于基态或处于激发态的场,都可以与其他的场发生相互作用;粒子间的相互作用和转化,乃是场之间相互作用的结果。以 β− 衰变 n → p + e− + \({\bar \nu }\) 为例:开始时中子场处于激发态,表现为存在一个中子,而质子场、电子场和中微子场则处于基态,表现为没有质子、电子和中微子。经过中子场与质子场、电子场和中微子场的弱相互作用,中子场跃迁到基态,由于能量的传递使质子场、电子场和中微子场受到激发,表现为中子消失而产生了一个质子、一个电子和一个反中微子。这就是通过弱相互作用的 β− 衰变的量子场论图景。
在粒子世界里,除了强相互作用、电磁相互作用和弱相互作用外,有迹象表明,可能还有超弱相互作用与超强相互作用存在。某些相互作用间可能有本质的联系,可以统一理解。例如,已由实验证实的弱电统一理论,就把弱相互作用和电磁相互作用作了统一的解释。还有大统一理论和超统一理论,则企图在更广泛的范围内统一理解各种相互作用的本质。这些方面的理论和实验工作都在进行中。
10.太阳里的热核反应
热核反应在宇宙中是普遍的现象。在太阳和许多行星内部,温度都高达 1 000 万度以上,在那里热核反应剧烈地进行着。太阳内部,氢是最丰富的元素。太阳的热核反应是氢核聚变为氦核的过程,有两种可能发生的反应序列:一种是质子循环,另一种是碳氮循环。
质子循环的反应如下:
11H + 11H → 21H + 01e
11H + 21H → 32He
32He + 32He → 42He + 211H
前两个反应,在生成 42He 核时都必须进行两次。
碳氮循环的反应如下:
11H + 126C → 137N
137N → 136C + 01e
136C + 1H → 147N
147N + 11H → 158O
158O → 157N + 01e
157N + 11H → 126C + 42He
两种循环都是 4 个质子聚合成一个 42He 核,释放出两个正电子。正电子跟电子相遇,发生湮灭,转变为 γ 光子。每个反应序列都放出约 28 MeV 的能量。两个序列发生的概率大致相等。
在太阳内部的热核反应中,每秒钟可将约 6 亿吨的氢变为氦,失去 400 多万吨的质量,释放的能量达 3.8×1026 J。太阳已燃烧了近 50 亿年。
11.核电池
将放射性核素辐射的核能转变成电能的装置,有以下几种不同的类型。
恒流充电型 β 放射性源放出的电子,给绝缘导体充电后被收集器收集起来。放射性源一端失去电子成为正极,收集器一端得到电子成为负极,在正负极之间形成电势差。这种核电池可产生高达 150 kV 的电压,但电流很小,最大短路电流只有 10−11 A。
温差电偶型 用放射线的能量给温差电偶的一个结点加热升温,得到温差电。实际装置是用一层转换体把放射性源包起来,转换体外面还有一绝缘层。转换体吸收了全部放射性粒子的能量,把核能转变为内能,温差电偶的热结点与转换体接触,其温度 Th 与转换体温度相同,外端的温度为 Tc,最大效率为 η = \(\dfrac{{{T_{\rm{h}}} - {T_{\rm{c}}}}}{{{T_{\rm{c}}}}}\)。
接触电势差型 把具有接触电势差的两个电极经由电阻连接起来,用放射性源发出的射线使电极间的气体电离,就可产生电流。
PN 结型 与光电池原理类似,用放射线照射 PN 结,产生电子—空穴对,在自建电场的作用下,空穴移向 P 区,电子移向 N 区,从而在 P 区和 N 区间产生电势差。
可用于核电池的核素有许多种,最常用的有两种:一种是经济易得的 90Sr(T1/2 = 28.5 a),一种是半衰期长、易于防护的 238Pu(T1/2 = 87.75 a)。
核电池具有结构紧凑,运行可靠,不受周围环境影响,能长期工作而无须看管等优点,可用于宇宙航行,空间考察,海上灯塔,海底电缆(增音器),沙漠、高山和险滩中的自动气象站、地震观测站等,5 ~ 10 年不需更换电源。医用的心脏起搏器也要使用核电池。
发布时间:2025/9/25 16:42:17 阅读次数:419