第十章 3 热力学第一定律 能量守恒定律
热力学第一定律
焦耳的实验一方面表明,以不同的方式对系统做功时,只要始末两个状态是确定的,做功的数量就是确定的;另一方面也向我们表明,为了改变系统的状态,做功和传热这两种方法是等价的,也就是说,一定数量的功与确定数量的热相对应。
在焦耳之前,人们还没有认识到做功与传热在改变系统内能方面是等价的;焦耳做实验的本意是要探究两者的关系。
我们在前两节已经指出,单纯地对系统做功和单纯地对系统传热,内能的增量与功、热量的关系分别是ΔU=W和ΔU=Q。既然做功与传热在改变系统内能方面是等价的,那么当外界既对系统做功又对系统传热时,内能的增量就应该是
ΔU=Q+W
也就是说,一个热力学系统的内能增量等于外界向它传递的热量与外界对它所做的功的和。这个关系叫做热力学第一定律(first law of thermodynamics)。
思考与练习
一定量的气体,膨胀过裎中是外界对气体做功还是气体对外界做功?如果膨胀时做的功是135 J,同时向外放热85 J,气体内能的变化量是多少?内能是增加了还是减少了?
请你通过这个例子总结ΔU、Q、W几个量取正、负值的意义。
能量守恒定律
过去我们学过了机械能守恒定律,其实那只是普遍的能量守恒在机械能范围内的表现。
能量守恒定律不是由某一个人通过某一项研究而得到的。从18世纪末到19世纪40年代,不同领域的科学家从不同角度都提出了能量守恒的思想。人类对于能量守恒的认识经历了一个由浅入深、由含糊到清晰的过程。
俄国化学家盖斯于1 836年发现,任何一个化学反应,不论是一步完成,还是分几步完成,放出的总热量相同,这表明一个系统(即参加化学反应的几种物质)存在着一个与热量相关的物理量,在一个确定的化学反应中这个量是不变的。这一发现被认为是能量守恒定律的先驱。
德国医生J.R.迈尔任船医时,在热带地区看到海员静脉中的血比在欧洲时更红,他联系到A.L.拉瓦锡的燃烧理论,认为在热带时人体会从外界获得一些热量(或说人体向外界散发的热量较少),因而机体需要从食物获得的热量较少,食物氧化过程减弱,静脉血中留下较多的氧,显红色。他由此想到食物中化学能与热能的等效性。迈尔还从海员谈话中听到海水在暴风雨中较热,于是想到热与机械运动的等效性。他在1841年和1842年连续写出论“自然力”(指能)守恒的论文,并推算了多少热与多少功相当。因此,迈尔是公认的第一个提出能量守恒思想的人。
以现代科学的观点看,迈尔的推理未必经得起推敲。但正是这些根据不充分的事实、经过不严格的推理而得出的“猜想与假设”,才是创造性思维中的最活跃的因素。
以上思想说明,这些人已经朦胧地意识到不同形式的运动之间可以相互转换,转换过程中某个物理量可能是不变的,但还没有定量的描述。焦耳的实验精确地测量了做功与系统状态变化之间的关系,也就是精确地测量了做功与传热之间的等价关系,从而为能量守恒定律奠定了牢固的实验基础。
德国科学家H.亥姆霍兹在不了解迈尔和焦耳的研究的情况下,从永动机不可能制成这一事实出发,考察了自然界不同的力(指不同的能)之间的相互关系,提出了“张力”(即势能)与“活力”(即动能)的转换。他还分析了在电磁现象和生物机体中能的守恒问题。此外,还有好几位科学家对这条定律作出了贡献。
能量守恒定律(law of energy conservation)可以表述为:能量既不会凭空产生,也不会凭空消失,它只能从一种形式转化为另一种形式,或者从一个物体转移到别的物体,在转化或转移的过程中其总量保持不变。
能量守恒定律告诉我们,各种形式的能可以互相转化。燃料燃烧生热,化学能转化成内能;在吸热反应中,内能转化为化学能;在发电机和电动机里,电能与机械能相互转化;电灯发光时,电能转化为光能;蓄电池充电和放电时,化学能与电能相互转化;各种生物电、生物磁现象,则是生物体内的化学能与电磁能的相互转化……事实表明,在所有这些转化过程中,能量都是守恒的。
以焦耳的实验为基础的热力学第一定律,实际上就是内能与其他能量发生转化时的能量守恒定律。
在20世纪30年代初,W.泡利和E.费米根据能量守恒定律预言了中微子[1]的存在并在后来得到证实。
能量转化和守恒定律的发现是科学史上的重大事件。恩格斯把它与细胞学说、生物进化论一起列为19世纪的三大发现。
能量转化和守恒定律的意义在于它把原来人们认为互不相关的各种现象——力学的、热学的、电学的、磁学的、光学的、化学的、生物学的、地学的——联系在一起,把表面上完全不同的各类运动统一在一个自然规律中。这样,它就使不同领域的科学工作者有了一系列的共同语言。现在,能量守恒定律仍然是我们研究自然科学的强有力的武器。
永动机不可能制成
17~18世纪,即资本主义发展初期,为了满足生产对于动力日益增加的需求,许多人致力于制造一种机器,它不需要任何动力或燃料,却能不断地对外做功,史称“第一类永动机”。然而,为此目的的任何尝试都失败了。为什么呢?答案就在能量守恒定律之中。
为什么叫做“第一类永动机”?下面一节我们就会看到,还有第二类永动机。
任何动力机械的作用都是把其他形式的能转化为机械能。内燃机把燃料的化学能转化为燃气的内能然后再转化为机械能,电动机把电能转化为机械能……如果没有燃料、电流或其他动力的输入,能量从哪里来呢!永动机的思想违背了能量守恒定律,所以是不可能制成的。
应该指出的是,制造永动机的千万次失败使人们的头脑冷静下来,开始在更深层次寻找失败的原因。1775年法国科学院宣布“不再审查有关永动机的一切设计”。这使得人们走出迷梦,去研究各种能量形式相互转化的规律,促成了能量守恒定律的建立。我国物理学家冯端教授[2]指出:除了要为焦耳、亥姆霍兹和迈尔这些做了杰出贡献的科学家树碑立传外,还应建立一个无名英雄纪念碑,其上最合适的铭文将是“纪念为实现永动机的奋斗而失败的人们”,这是因为人类在探索自然规律的过程中必然有各种假设,虽然后来发现某些假设是错误的,但正是前人的失败才使后人的思考走上了正路。
历史上设计永动机的人们以自己的失败帮助我们找到了正确的方向;他们的不懈努力反映了人类追求幸福生活的美好愿望。后人不应该讥笑他们。
但是,今天我们知道了能量守恒定律,就不要在这类徒劳中浪费时间了。
说一说
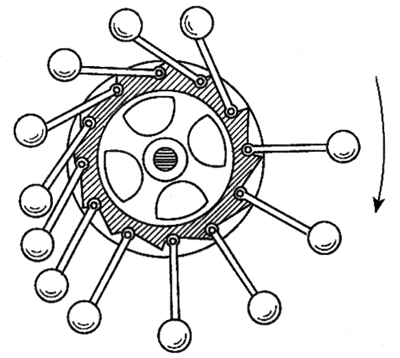
图10.3-1是历史上有名的一种永动机的设计。从图上看,设计者为什么认为这个机器会永远运动下去?不用能量的概念,你能不能说明它不会永远运动下去?
问题与练习
1.用活塞压缩汽缸里的空气,对空气做了900 J的功,同时汽缸向外散热210 J,汽缸里空气的内能改变了多少?
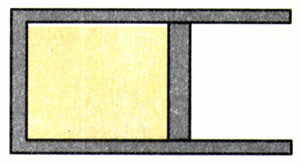
2.如图10.3-2,在汽缸内活塞左边封闭着一定量的空气,压强和大气压相同。把汽缸和活塞固定,使汽缸内空气升高一定的温度,空气吸收的热量为Q1。如果让活塞可以自由滑动(活塞与汽缸间无摩擦、不漏气),也使汽缸内空气温度升高相同温度,其吸收的热量为Q2。
(1)Q1和Q2哪个大些?
(2)气体在定容下的比热容与在定压下的比热容为什么会有不同?
3.为测算太阳射到地面的辐射能,某校科技实验小组的同学把一个横截面积是300 cm2的矮圆筒的内壁涂黑,外壁用保温材料包裹,内装水0.6 kg。让阳光垂直圆筒口照射2 min后,水的温度升高了1℃。请由此估算在阳光直射时地面上每平方米每分钟接受的太阳能量。
4.某风景区有一处约20层楼高的瀑布,甚为壮观。请估计:瀑布上、下水潭的水温因瀑布的机械能转化成内能而相差多少?
5.奶牛的心脏停止跳动后,大约在1 h内体温由37.0 ℃降低到33.5 ℃。请你由此估算,在这种环境下饲养奶牛,要维持一个体重400 kg奶牛的内能不变.每天喂养奶牛的食物至少要能为它提供多少热量?计算时,可以认为奶牛体内绝大部分为水。
6.如果用Q表示物体吸收的能量,用W表示物体对外界所做的功,AU表示物体内能的增加,那么热力学第一定律可以表达为Q=ΔU+W。怎样解释这个表达式的物理意义?
[1] 中微子是静止质量几乎为零的中性粒子,我们在《选修3-5》中还会遇到它。
[2] 冯端(1923~ ),南京大学物理系教授,中国科学院院士,曾任中国物理学会理事长。主要研究方向为凝聚态物理学。引文见《熵》,科学出版祉1992年第1版。
发布时间:2017/6/2 7:53:14 阅读次数:4366