第十二章A 原子的核式结构
线度大致大于10-7m的物质常称为宏观物质。宏观物质世界中的物理现象可用经典物理学描述。线度大致小于10-8m的粒子,如分子、原子、原子核等,常称为微观粒子。另一方面,线度大于星系的物质可称为超宏观或宇观物质。微观和宇观世界与我们生活的宏观世界一样丰富多彩,但其中的规律性却有很大的不同。20世纪物理学在这两个领域的进展极大地拓展了人们的视野,增强了人类认识和利用自然的能力。
本篇中你将初步了解微观和宇观世界中客观物质的某些特性,了解人类对它们的探索历程。
导学
在本章中,你将学到:
- 原子的结构式怎样的?
- 如何探测物质的放射性?
- 原子核由什么组成?
- 怎样获得核能?怎样和平利用核能?
天然放射性现象的发现,开创了人类探索微观世界的新时代。利用放射性,可以确定生物体遗骸的年代,这种方法称为放射性鉴年法。图12-1所示的这块琥珀中的小昆虫,用放射性鉴年法测出它大约生存在5000年前。

为了深入研究物质的微观构造,科学家们设法“撞开”了原子核,经过长期的努力,不仅揭示出原子核内部的奥秘,还发现了新的能量形式——核能。
核能是蕴藏在原子核内部的能量。核电站是利用核能转变为电能进行发电的发电厂。我国自行设计、建造的第一座核电站——秦山核电站(图12-2),总装机容量达2.9×106kW。秦山核电基地的建成,结束了我国有核无电的历史,成为我国和平利用核能的典范。

人类生活在丰富多彩的物质世界中,享受着大自然的“恩宠”。同时,人们也在不断地探索:物质究竟是由什么组成的?它的微观结构又是怎样的?
很早以前,人们就有了物质组成的观念:物质由分子构成,分子又由原子组成。“原子”这一术语来自希腊文,它的涵义是“不可分割的”。但是,不管是在古希腊还是古代中国,都有人提出相反的观点,他们认为物质是无限可分的。1897年,英国物理学家汤姆孙(J.J.Thomson,1856—1940)发现了电子,使人们进一步认识到原子不是组成物质的最小单位,它是有内部结构的。
大家谈
将如图12-3所示的阴极射线管接通高压直流电源,可以看到管内阴极发射出一束射线,使涂有荧光物质的白色底板上出现一条亮迹。那么,阴极发射出的究竟是什么射线呢?

科学家通过对这个实验现象的研究,拉开了探索物质微观结构的序幕。
阴极发射的是什么射线?
在图12-3所示的实验中,我们看到了在白色底板上的亮迹,这表明阴极发出了射线,并且射线是沿直线传播的。人们把这种从封装在真空玻璃管中的阴极发出的射线称为阴极射线,能产生阴极射线的管子称为阴极射线管。那么,阴极射线的本质又是什么呢?
1897年,汤姆孙通过一系列关于阴极射线的实验,得出了如下的结论:阴极射线是由质量小于一个氢原子质量的千分之一、带负电的粒子组成的。他把这种粒子定名为“电子”。电子是原子的组成部分。
1.电子(electron)的发现
电子的发现证实了原子是可分的。电子是原子的组成部分。
电子是质量m=9.1×10-31kg、电荷量大小e=1.6×10-19C、带负电的粒子。
汤姆孙的发现打破了传统的“原子不可分割”的旧观念,并使人类认识了第—个比原子小的微观粒子——电子。从此,人类对原子内部结构的探索开始了新的历程。汤姆孙为此荣获了1906年诺贝尔物理学奖。
原子的内部结构是怎样的?
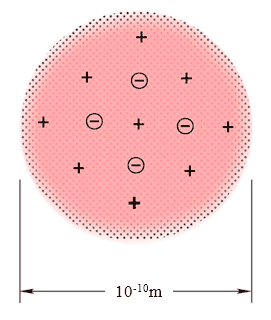
既然电子是原子的组成部分,带负电荷,而原子是呈电中性的,这表明原子内部还有带正电荷的物质,而且正、负电荷量大小是相等的。
当然,原子的内部结构想用肉眼看是不可能的。在20世纪初,即使凭借当时最先进的显微镜也做不到。好在人类洞察自然的本领与手段并不只局限于一个“看”字,人们可以根据已知的实验事实,提出假说与物理模型,去模拟所研究的客体。
20世纪初期,科学家们对原子的结构提出了多种不同的原子结构模型。例如,1904年汤姆孙首先提出了原子的“葡萄干蛋糕模型”(图12-4),该模型提出:原子的正电荷和质量均匀分布于原子体内,带负电的电子镶嵌在原子体内。如果将原子比作蛋糕,那么电子就如同散布在蛋糕中的葡萄干。
为了检验汤姆孙提出的原子结构模型,1909年,英国物理学家卢瑟福(E.Rutherford,1871—1937)和他的同事们用高速飞行的α粒子去轰击金箔,根据α粒子飞行路径的改变,来探测靶原子(金原子)的构造情况。图12-5是实验装置示意图。
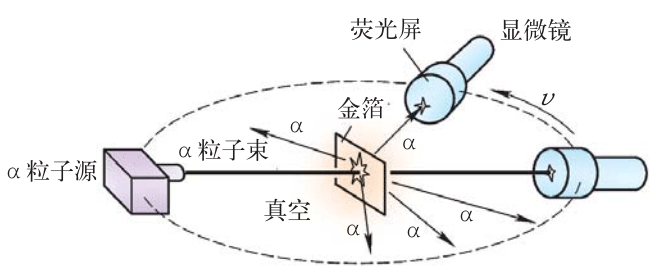
2.原子(atom)核式结构模型的提出
卢瑟福通过α粒子散射实验,否定了汤姆孙的无核原子结构模型,提出了原子核式结构模型。
实验的结果是:
(1)绝大多数α粒子穿过金箔后,与原来的运动方向偏离不多(平均2°~3°)。
(2)少数α粒子产生较大角度的偏转。
(3)极少数α粒子产生超过90°的大角度偏转,个别α粒子甚至被弹回。
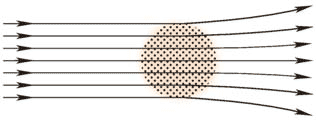
α粒子是带正电的,它的偏折是由于受到原子内正电荷的排斥而发生的。根据汤姆孙的“葡萄干蛋糕模型”,正电荷均匀地充满了原子内部,因此所引起α粒子的偏转效果根本不可能产生大角度、甚至大于90°的偏转(图12-6);再说,α粒子的质量约为电子质量的7300倍,如果碰到原子中的电子,就好似一颗枪弹碰上了一粒灰尘,也不会引起明显的偏转。因而,卢瑟福的α粒子散射实验使汤姆孙的模型陷入了困境。
卢瑟福在相同条件下,用不同金属的箔片作为靶进行多次实验,观察到的实验结果基本相似。
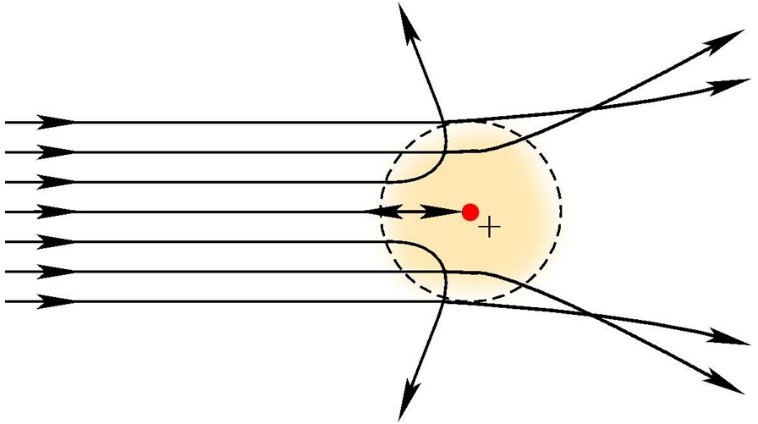
1911年,卢瑟福在α粒子散射实验结果的基础上提出了原子核式结构模型(又称为“行星模型”)。根据他的理论,原子的正电荷集中在原子中央很小的体积内,这些集中的正电荷对α粒子的排斥力可能非常大,以至α粒子发生较大角度的偏转(图12-7)。他还定量计算了偏转角与入射α粒子数、α粒子能量的关系。
1913年,他的学生盖革和马斯登用实验证实了这个关系。
从此,卢瑟福的原子核式结构模型很快被人们所承认。
从汤姆孙模型发展到卢瑟福模型,标志着人类对原子结构的认识迈出了一大步。
根据卢瑟福的原子核式结构模型可知,原子中绝大部分是空的,原子核显得非常小,其半径只有原子半径(原子半径数量级为10-10m)的十万分之一。

3.卢瑟福的原子核式结构
(1)在原子中心有一个很小的核,叫做原子核。
(2)原子的全部正电荷和几乎全部质量都集中在原子核里。
(3)带负电的电子在核外不停地绕核运动(电子绕核运动所需的向心力就是原子核对它的电场力)
拓展联想
从核式结构模型到量子力学
卢瑟福的核式结构模型较好地解释了少数α粒子发生大角度偏转问题。但是根据经典电磁理论,这样的原子结构是不稳定的。为了解决这个矛盾,丹麦物理学家玻尔在卢瑟福核式结构模型的基础上,结合普朗克的量子理论,建立了玻尔原子模型。这个原子模型在解释氢原子光谱时取得了相当的成功,但是它有着一系列难以克服的困难,例如它不能解释只比氢原子多一个核外电子的氦原子光谱等。这导致了描述微观粒子运动规律的基本理论——量子力学的发展。量子力学告诉我们,所谓核外电子运行的“轨道”只表示电子在核外的“轨道”处出现的概率较大。
点击
原子光谱
原子的稀薄气体或金属的蒸气发出的光经色散后成为由一系列波长不同的单色光组成的细条纹,这就叫做光谱。光谱中每一条条纹叫做谱线。每一种游离状态的原子发射的光谱由特定的一系列不同波长的谱线组成,我们把这种光谱叫做原子光谱。
文件下载(已下载 141 次)发布时间:2016/9/1 下午1:06:20 阅读次数:1911
