七、气体分子运动的特点
分子间的距离较大 气体很容易被压缩,说明气体分子间的距离比较大。气体凝结成液体时,体积要缩小上千倍,而液体不容易被压缩,可以认为其中的分子几乎是紧密排列的,可见气体分子之间的距离大约是分子直径的\(\sqrt[3]{{1000}}\)倍,即10倍。由于气体分子间的距离比较大,所以在处理某些问题时可以把气体分子看作是没有大小的质点。也是由于气体分子间的距离比较大,分子间的相互作用力十分微弱,所以通常可以认为,气体分子除了相互碰撞或者跟器壁碰撞外不受力的作用,可以在空间里自由移动。由此可以说明:气体能充满它所能达到的空间,既没有一定的体积,也没有一定的形状。
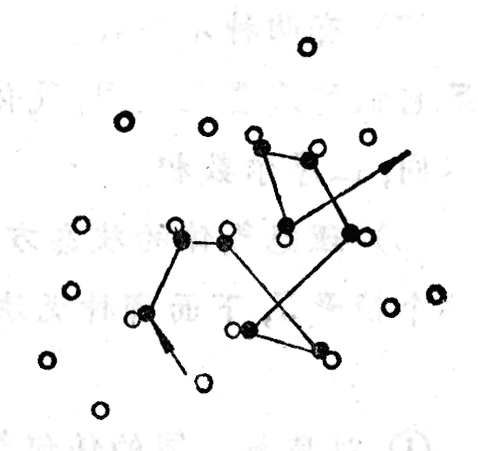
分子间的碰撞频繁比起固体和液体来,气体中的分子是比较稀疏的,但是单位体积中的分子数还相当大。在标准状态下,1厘米3气体中仍含有2.7×1019个分子。大量分子永不停息地运动,分子之间不断地发生碰撞。在标准状态下,一个空气分子在1秒内与其他空气分子的碰撞竟达65亿次之多。频繁的碰撞使得每个分子的速度的大小和方向频繁地改变。设想我们追随某个气体分子的运动(图3-13),我们将看到这个分子的运动是忽左忽右,忽前忽后,时快时慢,运动轨迹是一条极不规则的折线,频繁的碰撞造成气体分子做杂乱无章的热运动。
通常假定分子之间或分子与器壁之间的碰撞是完全弹性碰撞。
分子沿各方向运动的机会均等 气体分子做杂乱无章的热运动,就某一个分子来说,它在某一时刻的速度具有怎样的大小和方向,完全是偶然的。但是,对大量分子的整体来说,分子的运动却表现出一定的规律。先来讨论分子运动的方向,正因为大量分子的运动十分混乱,在某一时刻向任一方向运动的分子都有,因而可以想见,在任一时刻分子沿各方向运动的机会是均等的,没有任何一个方向,沿着它运动的分子的数目更多。设想真有这么一个方向,那么,由于气体分子的频繁碰撞,分子的运动越来越混乱,这个方向也不会存在了。这就是说,气体分子沿各个方向运动的数目应该是相等的。
这里所说的数目相等,是对大量分子用统计方法得到的一个统计平均数,与实际数目会有微小的出入。分子数越多,这种用统计方法得到的结果跟实际情况越符合。用分子运动论的观点研究热现象,涉及的总是大量分子,统计方法非常有用。
分子速率按一定规律分布 大量分子傲无规则运动,速率有的大,有的小,但分子的速率却按照一定的规律分布。
研究表明,气体的大多数分子,速率都在某个数值附近,离开这个数值越远,分子数越少,表现出“中间多,两头少”的分布规律。下表是氧气分子速率的分布情况。我们看到,在0℃时速率在300~400m/s这一速率区间的分子数最多,速率大干400m/s和小于300m/s的分子数依次递减,速率很大和很小的分子实际上很少。温度升高时,这种“中间多,两头少”的分布规律虽然不变,可是与分子数的最大值相对应的速率区间却移向速率大的一方,也就是说,温度升高时,速率小的分子数减少,速率大的分子数增加。这种速率分布规律是一种统计规律。表中的在某一速率区间的相对分子数,也是对大量分子用统计方法得到的统计平均数,与实际数值会有微小的出入。
|
按速率大小划分的区间(m/s) |
各速率区间的分子数占总分子数的百分率(%) |
|
|
0℃ |
100℃ |
|
|
100以下 |
1.4 |
0.7 |
|
100~200 |
8.1 |
5.4 |
|
200~300 |
17.0 |
11.9 |
|
300~400 |
21.4 |
17.4 |
|
400~500 |
20.4 |
18.6 |
|
500~600 |
15.1 |
16.7 |
|
600~700 |
9.2 |
12.9 |
|
700~800 |
4.5 |
7.9 |
|
800~900 |
2.0 |
4.6 |
|
900以上 |
0.9 |
3.9 |
既然在一定温度下,某种气体的分子速率分布是确定的,我们就可以求出在这个温度下该种气体分子的平均速率。即所有分子的速率的平均值,温度升高时,速率大的分子数增加,分子的平均速率增大。例如氮气分子的平均速率在-150℃时为305m/s,在0℃时为454m/s,在1000℃时为981m/s。这里我们又一次看到,温度越高,分子的热运动越激烈。
文件下载(已下载 54 次)发布时间:2015/8/25 12:58:24 阅读次数:3488